Na mesma semana em que o Brasil e o mundo ultrapassam diariamente os seus próprios recordes de novos casos diagnosticados de covid-19, o Ministério da Saúde e a Anvisa (Agência Nacional de Vigilância Sanitária) travam uma batalha sobre testes para diagnóstico dessa infecção.
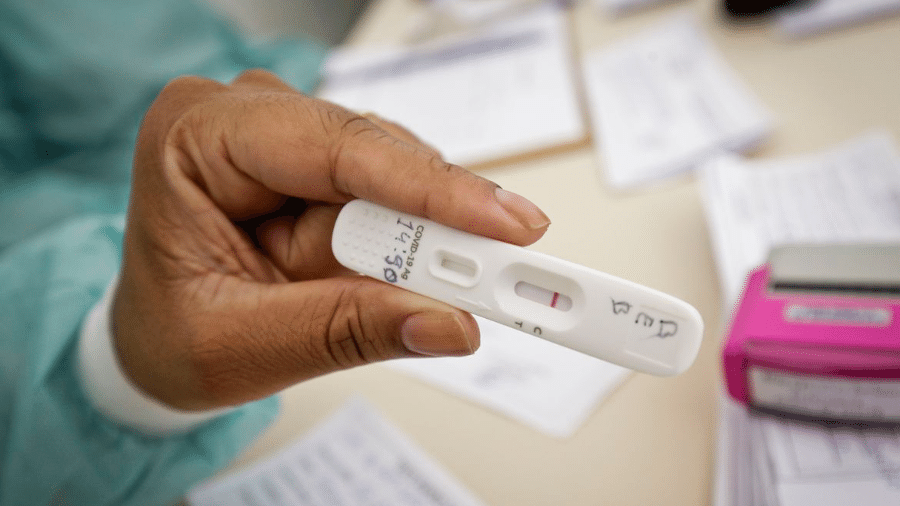
No centro do debate está a liberação do uso domiciliar de testes rápidos de antígeno, dispositivos para uma testagem realizada e interpretada pelo próprio usuário, capazes de identificar com sensibilidade satisfatória (e em apenas 15 minutos) os casos de infecção por coronavírus.
Enquanto na América do Norte e na Europa esse tipo de teste já faz parte da estratégia de controle da pandemia e é amplamente utilizado, o enrosco brasileiro está numa resolução de 2015 da Anvisa, que proíbe que dispositivos para diagnóstico de doenças transmissíveis passíveis de notificação compulsória sejam distribuídos ou utilizados pela população leiga, restringindo o seu uso apenas por serviços ou profissionais da saúde.
A restrição imposta pela resolução existe para evitar que esses testes sejam realizados ou tenham seus resultados interpretados de forma equivocada, no entanto quem já utilizou um autoteste de covid-19 logo percebeu que todos os procedimentos são bastante simples e de fácil realização.
A mesma resolução já tinha sido questionada em 2016, quando se discutia a liberação do autoteste de HIV no país. Depois de um longo debate sobre o tema, a compreensão na época foi a de que para o Brasil atingir as metas propostas pelo Unaids (Programa Conjunto das Nações Unidas sobre HIV/Aids) de controle dessa epidemia, seria preciso ampliar o acesso à testagem e ao diagnóstico da infecção por HIV. Era preciso fazer a testagem de HIV chegar aonde não estava chegando.
Com essa argumentação, foi aberta a primeira exceção à resolução da Anvisa. Entretanto, a liberação do uso do autoteste de HIV foi condicionada a uma série de exigências, como a disponibilização de uma linha permanente de atendimento ao usuário com orientações sobre os procedimentos da testagem, interpretação do resultado e encaminhamento, caso positivo, para um serviço de saúde para confirmação do resultado.
Atualmente, kits de autoteste de HIV são distribuídos gratuitamente em todo país para a população mais vulnerabilizada à essa epidemia, dentro do programa brasileiro de HIV/Aids. De acordo com as estimativas do último Relatório de Monitoramento Clínico de HIV/Aids do Ministério da Saúde, entre 2012 e 2020, a proporção de pessoas infectadas com HIV no país que já tinham se testado e feito o diagnóstico da sua infecção subiu de 69% para 88%. A meta do Unaids era 90%.
Na mesma linha, um estudo conduzido pela Faculdade de Medicina da USP e publicado no ano passado demonstrou que, entre indivíduos vulneráveis à infecção por HIV do município de São Paulo, os que mais se interessavam pela autotestagem eram justamente aqueles que nunca haviam se testado na vida.
HIV e coronavírus são dois vírus com características, vias de transmissão e epidemias com dinâmicas completamente diferentes, mas independente do vírus em questão, sabemos que obstáculos à testagem sempre vão favorecer a sua disseminação.
Enquanto para o HIV os obstáculos à testagem são o estigma e o preconceito associados à doença, para a covid-19 o principal obstáculo nesse início de ano é a disponibilidade de testes. Com a explosão de casos provocada pela variante ômicron, os serviços de saúde têm longas filas para atendimento, enquanto farmácias e laboratórios não conseguem dar conta da alta demanda de testes.
O desabastecimento dos testes de covid-19 foi tanto que na última semana a Abramed (Associação Brasileira de Medicina Diagnóstica) propôs que fossem testados apenas os casos graves de covid-19, que precisassem de internação hospitalar. Se essa medida fosse adotada, seria o fim da contagem dos casos e da tentativa de controle da epidemia.
Por outro lado, a liberação do uso de autotestes, depois de uma validação adequada, ampliaria o acesso à testagem para covid-19 para os casos leves, permitindo a rápida tomada de medidas de isolamento e reduzindo a circulação do coronavírus na comunidade.
Mas liberar o uso de autotestes de covid-19 não pode ser apenas permitir a venda. Segundo Carolina Lázari, médica chefe da Seção de Biologia Molecular do Laboratório Central do HCFMUSP, “a incorporação de autoteste de covid-19 deve ser acompanhada de uma estrutura de notificação e de monitoramento dos casos, além de um programa estruturado de saúde pública, com distribuição gratuita dos kits e educação para população sobre o que fazer no caso de um teste positivo. Apenas colocar o autoteste na prateleira da farmácia pode atrapalhar mais que ajudar”.
Depois de um pedido do Ministério da Saúde de liberação dos autotestes negado pelos diretores da Anvisa, em 2 semanas um segundo plano deve ser avaliado pelos técnicos da agência. Nesse segundo pedido, esperamos que o Ministério da Saúde leve em conta a experiência brasileira com o autoteste de HIV e conhecimento de especialistas na área, e não simplesmente utilize o tema como forma de terceirizar a sua responsabilidade no enfrentamento e controle da epidemia de covid-19.
Fonte: Viva Bem (UOL) / Coluna Rico Vasconcelos











