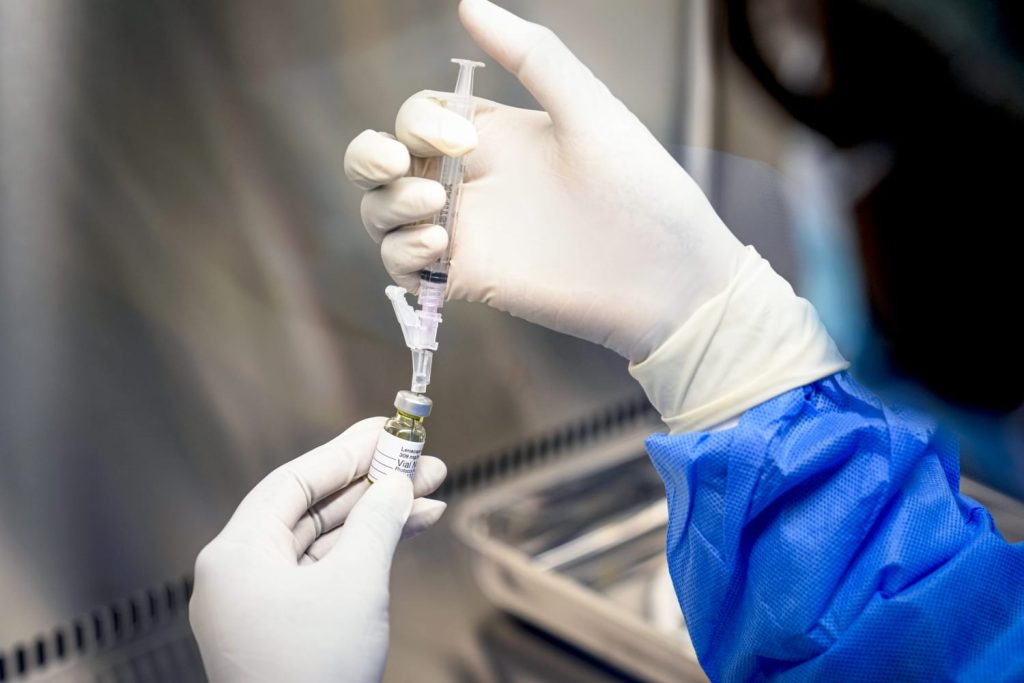
A aprovação do lenacapavir (Sunlenca) pela Agência Nacional de Vigilância Sanitária (Anvisa) para profilaxia pré-exposição (PrEP) contra o HIV representa um avanço científico relevante na resposta à epidemia. Com alta eficácia e aplicação semestral por injeção subcutânea, o medicamento amplia as possibilidades da prevenção combinada, especialmente diante dos desafios de adesão à PrEP oral diária.
No entanto, para ativistas da luta contra a aids, o registro sanitário está longe de significar acesso real. Questões como preço, patentes, monopólio farmacêutico e a incorporação ao Sistema Único de Saúde (SUS) colocam o lenacapavir no centro de um debate político que atravessa a soberania sanitária, o direito à saúde e o papel do Estado na resposta ao HIV.
A Agência Aids conversou com representantes da sociedade civil organizada. Confira o que eles disseram:
“Quando a inovação não chega a quem precisa, é preciso questionar se isso é, de fato, inovação”

Beto de Jesus, diretor da AHF Brasil, avalia que o registro do lenacapavir era esperado, mas alerta para o risco de o medicamento se tornar mais um símbolo de avanço científico inacessível:
“Já esperávamos por esse registro a qualquer momento. Agora podemos falar de algo mais prático em termos de timing de incorporação. No entanto, estamos diante de um avanço científico importantíssimo, cujo acesso ainda é distante.
Assim, sempre que estamos diante de uma inovação científica desta envergadura, mas ela é inacessível a quem mais precisa dela, devemos questionar se isso realmente é inovação.
O preço praticado nos EUA é 28 mil dólares paciente/ano, valor proibitivo ao SUS. Não nos esqueçamos que metade do orçamento de Dathi é drenado anualmente para outra bigpharma, a GSK, para o financiamento de uma mono droga, o DTG (Dolutegravir). Ao Brasil, resta, por ora, negociação a portas fechadas com a Gilead!
Precisamos recordar que o Brasil ficou de fora dos acordos de licença voluntária do lenacapavir da Gilead com 6 produtores para 120 países (alta carga de doença renda baixa). No entanto, o Brasil contribuiu com essa tecnologia em saúde, pois participou dos ensaios clínicos.
Ademais, a Gilead não levou em consideração a alta carga de doença no país, tampouco o financiamento público das políticas de HIV.
É preciso lembrar ainda que a licença voluntária continua boa para um lado, o mais forte, afinal, esse tipo de acordo não é mecanismo de acesso à saúde. É simplesmente uma transação comercial firmada entre o detentor da patente (neste caso a Gilead) e uma empresa que poderá produzir e comercializar a droga, porém, mediante cláusulas definidas pela Gilead. Ou seja, esse acordo mantém o monopólio e as iniquidades no acesso!
Há outro ponto supercrítico, mesmo diante do registro do lenacapavir na Anvisa: já temos 3 patentes do lenacapavir concedidas no Brasil. Com isso, estamos sob o monopólio da Gilead até 2037.
O Brasil poderia dar o bom exemplo, mais uma vez, e ditar o ritmo das negociações com a Gilead e da resposta de vanguarda ao HIV, como aconteceu no passado com o efavirenz: 1. temos capacidade tecnológica para produzir o lenacapavir (quiçá contribuir com a produção e oferta regional, o que defende a AHF), por meio de engenharia reversa – ou seja, há capacidade institucional; 2. Há o precedente histórico do efavirenz, único case de licenciamento compulsório (“quebra de patente” na linguagem mais palatável); 3. Já temos a sociedade civil mobilizada na dianteira; e 4. Temos forte influência regional.”
“Aprovação regulatória não é sinônimo de acesso”

Para a Rede Nacional de Pessoas Vivendo com HIV/Aids (RNP+Brasil), o debate central agora é garantir que o avanço científico se traduza em política pública.
Thiago Rodrigues, secretário político da RNP+Brasil, afirma:
“A RNP+ Brasil reconhece a liberação do lenacapavir como um avanço importante e necessário no enfrentamento da epidemia de HIV no país. A incorporação de tecnologias de longa duração na prevenção representa uma resposta alinhada às evidências científicas e às demandas históricas da sociedade.
A RNP+ Brasil destaca que a ampliação das opções de prevenção fortalece a autonomia das pessoas, e contribuí para estratégias mais eficazes, diversificadas e adequadas às realidades vividas por populações-chave e prioritárias. Contudo, ressaltamos que aprovação regulatória não é sinônimo de acesso, e um alerta para o risco de que o lenacapavir se torne um recurso restrito, aprofundando desigualdades já existentes.
Nesse sentido, a RNP+ Brasil defende de forma enfática a incorporação do lenacapavir no SUS, com financiamento público adequado, que garantam sua disponibilização em todo o território nacional.
O lenacapavir deve integrar as políticas de acesso e prevenção, ou seja, inclusiva e baseada em direitos humano, somente assim será possível transformar esse avanço em uma conquista real para a saúde pública brasileira e para a superação da epidemia de HIV/aids no país.”
“O acesso não é um favor, é uma estratégia de saúde pública”

Na avaliação de Liliana Mussi, vice-presidente do Fórum das ONGs/Aids do Estado de São Paulo, o lenacapavir enfrenta um dos principais gargalos da prevenção atual: a adesão ao uso diário de medicamentos.
“A aprovação do Lenacapavir (Sunlenca) pela Anvisa é um marco histórico na resposta ao HIV. Mais do que uma nova opção de PrEP, trata-se de uma tecnologia que enfrenta uma das maiores falhas da prevenção atual: a dificuldade de adesão à PrEP oral diária. Ao oferecer um esquema de longa duração, o Lenacapavir amplia o acesso à prevenção e melhora significativamente a qualidade de vida das pessoas.
O registro também contempla o uso no tratamento do HIV, trazendo esperança para pessoas que enfrentam falhas terapêuticas ou dificuldades de adesão aos esquemas existentes. No entanto, nenhuma inovação cumpre seu papel social se não chegar a quem precisa. Para ser incorporado ao SUS, o medicamento ainda precisa passar pela Conitec, que analisará critérios como eficácia, segurança, impacto orçamentário e custo-efetividade. O custo de tecnologias inovadoras é uma barreira global e seu alto custo não pode se tornar uma nova forma de exclusão.
O acesso não é um favor: é uma estratégia essencial de saúde pública. Governo, indústria e sociedade civil precisam construir, juntos, caminhos sustentáveis para garantir que essa inovação não aprofunde desigualdades, mas ajude a superá-las.”
Redação da Agência de Notícias da Aids
Dicas de entrevista:
Beto de Jesus
Instagram: beto.de.jesus
RNP+ Brasil
Site: www.rnpvha.org.br
Liliana Mussi
E-mail: liliana_jornalista@hotmail.com